介绍
本文旨在向 DMI-65 催化水过滤介质的用户提供有关材料工作原理、其能力和局限性的定性信息,并使他们能够以适当的方式和信心将材料应用于水处理过程。 避免了固体表面电化学层和胶体科学、定量物理和化学过程和反应的详细复杂性。 对于在这方面已经拥有重要知识的读者来说,本文可以更深入地了解什么是 DMI-65 及其预期用途。 该地区的新人得到了基地,也许还有动力,让他们按照他们所希望的那样指导他们更深入的研究。
历史
在水处理的早期,天然产生的沸石(如青石绿石)被用来软化和去除锅炉化妆和工艺水中的铁和锰。 随着对更高质量水的需求增加(部分由于压力等级锅炉),水处理行业基本上从这些产品转向软化,转向新开发的合成换水树脂。
然而,在铁和锰去除的情况下,这一举措要慢得多,结果是使用玻璃绿石和(绿色)过滤介质一直持续到现在。 Greensand 过去并且经常用作离子交换过程前的预处理步骤,因为给水中的铁可以并且会污染阳离子树脂。 其他工艺包括使用标准介质过滤器或专有类型的介质和/或过滤器进行曝气和氧化过滤
虽然有其他铁/锰去除产品和工艺开发自绿色和被引入使用绿色和继续,即使有几个问题,使其不太理想的媒体。 它需要与高锰酸钾的周期性再生,不能用于较低的pH水 < (6.2),工作温度相对较低(80oF),并倾向于软化随着时间的推移,导致压力下降问题在更高的流速。 此外,由于美国东海岸的加工设施受到环境问题的影响,供应可能偶尔受到限制。
由于这些问题,在20世纪70年代,水处理公司和最终用户开始表示有兴趣”别的东西”来取代绿色和。 为了满足他们的要求,日本的科学家和研究人员开始寻找方法,将氧化剂注入不同的基质材料中。 有人认为,商业生产的产品可以变得更强大,具有更好的物理性能,并更容易受到改进和/或修改比任何自然发生的介质。
数十年来,日本输液技术的进一步研究和开发,使独特的澳大利亚制造的产品,DMI-65粒催化介质用于提高水中先进的还原/氧化(氧化)过程。 该介质是广泛类别产品的一部分,它们的物理和化学作用来自其金属氧化物表面与溶液中的水分子和离子的相互作用。 本产品具有革命性,因为专有的输液技术可穿透基质材料的微浇注基板,从而获得更大的催化表面积和紧密的颗粒尺寸分布。 DMI-65 的罚款水平较低,pH 范围较宽,并且化学注入催化表面在正常操作条件下不会消耗或减少。 持续使用 5 – 10 年。
背景信息
DMI-65 是一种极其强大的催化水过滤介质,设计用于去除水溶液(水)中的铁和锰,无需高锰酸钾或化学再生。 DMI-65 独特的微孔结构可有效去除溶解铁,其水平几乎为 0.001 ppm,锰含量低至 0.001 ppm。 DMI-65作为氧化催化剂,立即氧化和过滤从这种氧化反应中获得的不溶性沉淀物。 DMI-65 还可在特定条件下去除砷、铝和其他重金属和硫化氢。
该材料是广泛类别产品的一部分,其物理和化学作用来自其金属氧化物表面与溶液中的水分子和离子的相互作用。
固体表面与水相互作用区分吸附物,即将疏水分子在刚性核心介质中(如活性炭和吸收)的弱范德瓦尔力区分开来,这种力将疏水性分子在可膨胀基质(如苯)中,或通过液体萃取吸收。 离子交换树脂利用吸收过程,而DMI-65与溶液中的水分子和离子的相互作用是通过吸附启动的。
非催化型吸附材料从水中保留目标离子,直到任何可用于吸附的位点达到处理水中目标离子的最大密度和饱和度或浓度,达到最大可接受的浓度。 此时,必须重新生成吸附材料以去除或更换污染物离子,或者将用过的材料替换为装载在处理容器中的新材料。 当该过程通过从水中交换一种类型的离子来交换目标离子时,该过程称为离子交换。 此类吸附剂和部分吸收性材料从水中去除目标离子。 每体积材料的表面越大,从水中保留的污染物目标离子量就越大。
纯催化材料吸附溶液中的活性离子,使其接近化学粘接。 然后反应产物远离催化剂表面。 严格地说催化剂有助于化学反应;它们不会隐式删除任何内容。 如果反应产物是固体沉淀物,则产品通常保留在催化床上,因此通过过滤将其去除。
许多材料在混合模式下工作;进行ion交换和催化作用。 对于主要用于催化作用的材料,导致催化层溶解的离子交换导致需要定期再生或重新活化以校正其活性表面的离子基质。
DMI-65 – 高级氧化催化介质
DMI-65 是深棕色到黑色的颗粒材料。 这种颜色是由颗粒外层中的氧化锰产生的。 DMI-65 是一种催化介质,具有该词的真正含义,有助于氧化 – 沉淀 – 过滤,不会在反应中消耗。 严格地说,介质有助于化学反应,不会明确去除任何内容。 氧化后,介质的深度过滤面会去除固体,然后定期从过滤容器中回洗。
介质不需要再生或重新激活,也不显示用于进行催化工作的衰变能力。 在5至10年的时间里,通过床的许多回洗操作来去除保留的固体,介质因颗粒接触和机械磨损而降解。 然后必须更换材料。
基本操作:
DMI-65 床中发生的过程涉及还原/氧化(氧化)。 雷血反应涉及物种之间的电子转移。 减少是电子的增益或分子、原子或电离的氧化状态的降低。 氧化是电子的丢失或分子、原子或电离的氧化状态的增加。 氧化反应同时发生,没有氧化反应,就不能产生还原反应。 介质通过与反应相互作用而不被永久改变而”帮助”化学反应的发生。 关于氧化还原化学的深入讨论不在本文的范围之内,它只会涉及氧化还原工艺如何应用于使用DMI-65去除铁和锰。 以下铁和锰去除部分将涵盖各个氧化还原方程。
为了开始溶液中离子的氧化过程,并确保氧化层不受损,介质设计为在存在氯或其他氧化剂的情况下运行。 在这个过程中,氧化剂去除电子,并在过程中消耗。 操作员需要确保污水中有 0.1 ~ 0.3 ppm 的游离氯残留。
氯,作为次氯酸钠(NaOCl)或漂白剂(12.5 NaOCl)喂养,是首选的氧化剂,因为它是相对便宜,在世界各地随时可用,并且是有效的。 其他氧化剂,如过氧化氢(H2O2)、氧化氯(ClO2)或臭氧,只要可以测量和维护残留物,也可以使用。
氯的另一个功能是,它使介质免受细菌或粘液的生长。 氧化锰催化表面必须保持清洁,以便水中的离子能够与它接触。 同时,氯是氧气的来源,比分子氧反应性更大。 下图指示可能干扰表面相互作用的其他水成分的安全水平。
与电离交换树脂不同,其中较高的再生剂剂量会增加电离交换能力,氯残差或浓度高于氧化Fe和Mn所需的浓度不会增加介质的氧化特性。 此外,由于介质通常用于在反向渗透 (RO) 系统之前预处理水,因此较高的游氯残留需要更广泛的后处理,以减少残留物以保护膜免受氯攻击。
在首次投入使用之前,必须激活 DMI-65。 这种激活需要比正常操作时使用的氯剂量更高,但在初始启动期间只需执行一次。 剂量率是10液体盎司12.5氯每立方英尺(英尺3)的介质。 激活只需要浸泡几个小时,但过夜浸泡是首选。
激活后,必须对容器进行回洗,以清除多余的 NaOCl 和任何罚款。 由于氧化锰是介质制造中使用的成分之一,因此在启动时需要延长冲洗,以去除制造过程中遗留下来的任何无痕锰氧化物残留物。 一旦回洗水中的 Mn 水平达到 0.05 到 0.15 ppm 的值,并设置游离氯残差,过滤器即可投入使用。
介质更换是由于介质的物理过滤性能降低,由于物理磨损,在催化层完全降解之前会发生。 在正常操作条件下,介质寿命估计为 5 – 10 年。
使用 DMI 65 进行铁 (Fe) 沉淀和去除
铁(Fe)是地壳中第四最常见的元素,在 -2 到 +6 的各种氧化状态中存在,尽管最常见的状态是铁(+2)和铁氧体 (+3)。
铁盐很容易溶解。 铁铁之前,一种溶解的固体,通常发现为碳酸氢盐铁,可以通过过滤去除,它必须被氧化,成为铁氧氢氧化剂和在中性pH水中沉淀在介质床。 DMI-65 的催化表面含有氧化锰或暴露锰和氧气位点,用于吸附 [Fe] 水中的离子。 碳酸氢铁和NaOCl的反应几乎是瞬时的,碳酸氢盐铁氧化(放弃OH-),成为不溶性铁氧氢氧化物,然后通过过滤在介质的催化表面去除。 以下氧化还原反应方程解释了该过程。
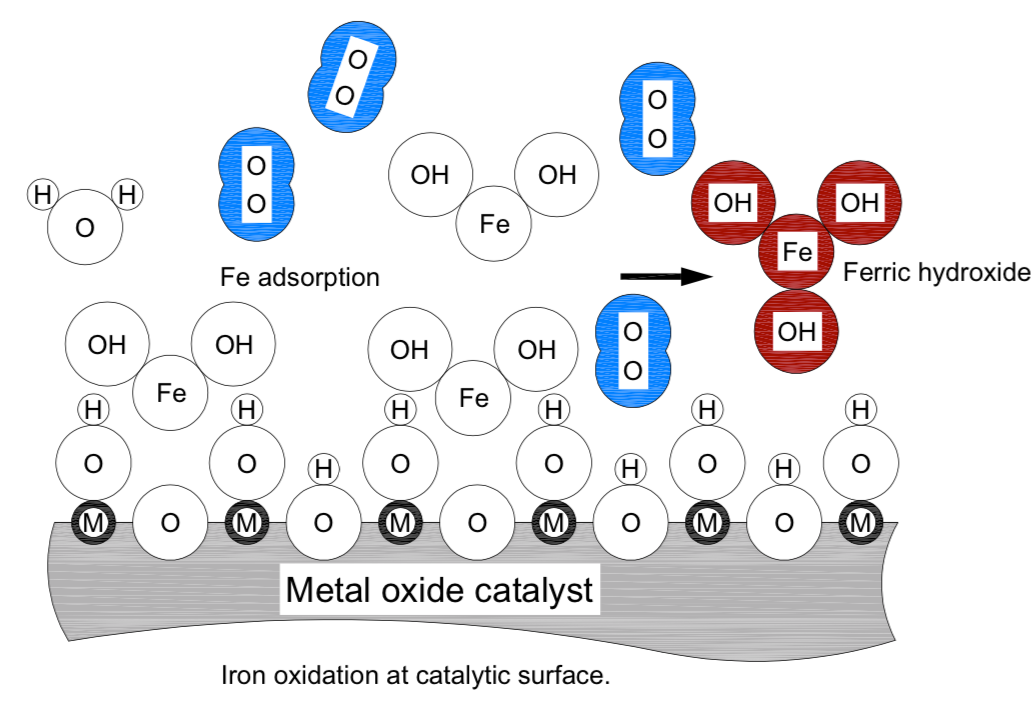
2Fe(HCO3)2 + NaOCl + H2O = 2Fe(OH)2 + 2CO2 = NaCl
在上图中,催化表面以简化的平滑形式呈现。 字母”M”用于表示该表面晶格中的通用金属 ion。 字母”O”,在圆圈的中心,代表一个氧原子。 各种ion大小和氧分子(蓝色)以真正的相对比例表示。 除氧分子外,粘结铁显示为切线圆。 图”催化表面离子氧化”中字母和离子的解释是:
M:催化表面晶格中的通用金属里昂(Mn+);n = 1, 2…
O:氧原子或Ion(O-)
铁原子或艾拉(Fe2+,Fe3+)
H:氢原子或Ion (H+)
OH:氢氧化铝或羟基阴烷(OH-)
H2O,水分子显示为切线圆
Fe (OH)2,氢氧化铁显示为切线圆
Fe (OH)3, 铁氧氢氧化铝,显示为切线圆,棕色
O2,氧分子,原子在共价粘合距离显示,蓝色
溶解的碳酸氢铁与铁端一起被吸引到催化材料的晶格氧上。 这使得Fe与邻近地点的氢氧化硅等值粘合接近,碳酸氢盐铁转化为不溶性氢氧化硅,以3纳米和更大的晶体形式沉淀成晶体。 聚合体在较大的羊群中凝固,并保留在催化床上。
当碳酸氢铁转化为铁氢氧化铁时,其催化表面的浓度降低。 在大部分水中,远离催化表面的碳酸氢铁浓度较高,因此根据扩散规律向低浓度扩散。 扩散通量与浓度梯度在距离上呈线性相关。
溶解氧通过直接氧化氢与Fe分裂水分子以及催化表面的氢反应,促进氢氧化离子的产生
需要注意的是,虽然需要氧气源氧化,而Fe的沉淀是由氢氧化ion驱动的。 即使在相对酸性条件下,氢氧化离子(一种非常强的离子)也比氧气更容易与Fe结合。 因此,Fe在中性pH条件周围氧化和沉淀并不难。 此外,羟基离子的浓度随着pH值呈指数级增长,Fe的氧化和沉淀率也呈指数级增长。
氯(通常以NaOCl的形式)是氧的来源,比分子氧反应性更大。 催化过滤器下游的理想残留为0.2毫克/升(0.1至0.3)自由氯。 催化过滤器中游离氯的残留率较高,因此次氯酸钠含量较高,并不总是有帮助的。 由于氯的排泄和竞争钠离子的增加,Na+可能会产生不良影响。 催化表面必须清洁,以便水中的离子能够与它接触,因此注入的氯也能防止细菌生长和用粘液使催化表面致盲。
锰,Mn沉淀和使用DMI65去除
DMI-65 是专为锰氧化和去除量身定制的催化材料。 催化表面含有锰氧化物,用于接近来自水中的共价粘接锰和氧原子。 然而,锰的氧化和去除(Mn)与Fe的氧化和去除有很大的不同。 一个主要的区别是由锰氧氢氧化铝(Oh)2的溶解性造成的。
Mn(HCO3)2 = NaOCl = MnO(OH)2 = NaCl = 2CO2
锰不沉淀为羟基氢氧化物,而是作为氧化物、MnO2和更高高的氧化物。 氢氧化阴离子的存在和浓度对锰的沉淀和去除没有多大帮助。 锰氢氧化剂将吸引锰端在催化晶格表面的氧气。 氧气分子必须靠近,以方便氧化通过氧气从晶格和交换到晶格与分子氧。 从统计学上讲,这种情况的可能性较小,反应速度比通过氢氧化剂氧化的Fe要慢得多。
虽然pH含量升高至碱性水平有助于氧化和去除锰,但在这些条件下,氧化锰也可以溶解回水中。 因此,无论要去除何种目标污染物,必须始终避免缺氧条件,以保护催化层不渗入水中。 氧化锰时,建议的pH接近8。
氧化锰具有良好的自催化作用。 反洗时,最好在水变得非常清澈之前停止处理过程。 过滤床上的氧化锰残留物将增强锰氧化。
关键 DMI-65 工作条件
处理过程必须以这种方式进行,以便材料的催化表面保持清洁,并且从水到接触的相声可用。
在使用 DMI-65 通过催化过滤器之前,必须澄清具有大量悬浮固体的水。 悬浮固体的可接受水平取决于其性质。 可以处理比有机悬浮固体更多的矿物悬浮固体。
细菌可以生长并沉积在DMI-65上。 因此,必须保持消毒和氧化条件。
含有粘土和大型有机分子的水可能导致此类材料沉积在DMI 65表面,并致盲催化表面。 在需要催化过滤器之前,对此类污染物进行去除处理。
聚合物絮凝物也可以粘到DMI-65和盲催化表面。
坚硬、不稳定的地下水可能导致催化过滤器中的水垢沉积,使材料在固体单体体体中致盲。 在这种情况下,床上的 DMI-65 材料丢失,必须更换。 必须进行稳定水以防止催化过滤器中形成垢的处理。
低酸性pH值和缺氧条件都可能导致DMI-65催化层锰溶解,并丧失其能力。 过高的pH值意味着氢氧化氢离子(对金属的腐蚀性)浓度过高,还可能导致锰从催化层溶解。
请勿使用脱矿水、蒸馏水或已知对金属具有强烈腐蚀性的水进行 DMI-65 的初始浸泡和激活。











